La energía es un recurso fundamental para todo ser vivo. Sin ella, ningún proceso biológico podría tener lugar, desde la contracción muscular y la transmisión nerviosa, hasta la síntesis de macromoléculas y la regulación de la temperatura corporal en organismos homeotermos.
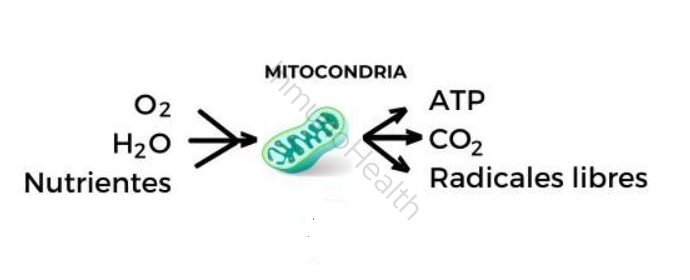
A nivel celular, la principal forma de energía química utilizable es el ATP (adenosín trifosfato), una molécula que sirve como “moneda energética” y facilita prácticamente todas las reacciones que requieren un aporte energético en la célula. Esta “moneda” se produce mayoritariamente en un orgánulo especializado: la mitocondria.
La producción de ATP no solo es un proceso bioquímico de interés académico, sino que impacta directamente en la medicina, la fisiología, la nutrición y la investigación farmacéutica. Cuando la producción de ATP es insuficiente o se ve alterada por alguna patología, pueden desencadenarse enfermedades degenerativas, desórdenes metabólicos y estados de fatiga crónica.
Por el contrario, optimizar la función mitocondrial se asocia con mejora en el rendimiento deportivo, la resistencia al estrés y la longevidad.
Ahora bien, a pesar de que las mitocondrias son las encargadas de producir grandes cantidades de ATP, este proceso no está exento de desafíos y riesgos. La producción de energía conlleva la generación de subproductos tóxicos como las especies reactivas de oxígeno (ROS), que pueden dañar proteínas, lípidos y ácidos nucleicos.
Para evitar un daño masivo y preservar la integridad celular, los organismos han desarrollado un sofisticado sistema de defensa antioxidante. Entre los protagonistas más destacados de este sistema se encuentra el glutatión, un tripéptido formado por tres aminoácidos (glutamato, cisteína y glicina) que desempeña un papel clave en la detoxificación y la homeostasis redox.
Este artículo busca ofrecer una visión completa de cómo se produce la energía en la mitocondria y, a la vez, profundizar en la función del glutatión como molécula esencial para mantener el equilibrio celular y apoyar el proceso bioenergético
Panorama histórico y relevancia de la bioenergética
La bioenergética estudia cómo las células obtienen y usan energía. Su desarrollo avanzó en el siglo XX con descubrimientos sobre la respiración celular, el metabolismo y, especialmente, el papel de la mitocondria en la producción de ATP.
Investigadores como Albert Lehninger y Peter Mitchell ayudaron a aclarar cómo funciona la cadena de transporte de electrones y la teoría quimiosmótica, que describe cómo la célula aprovecha los gradientes de protones para generar energía.
Al descubrirse que la mitocondria es el “motor energético” celular, se comprendió mejor su relación con diversas enfermedades.
Problemas en su funcionamiento se asocian a trastornos cardiovasculares y neurodegenerativos (por ejemplo, Parkinson o Alzheimer). También se encontró que la producción de energía genera radicales libres, lo que llevó a estudiar las defensas antioxidantes de la célula. En ese contexto, el glutatión cobró importancia por su capacidad de neutralizar esos radicales y proteger a la célula.
Hoy en día, gracias a la biología molecular y la bioquímica de sistemas, se conoce con más detalle cómo se produce el ATP y cómo se regulan los procesos de oxidación-reducción.
El estudio de la bioenergética mitocondrial y del glutatión sigue siendo clave tanto para entender la salud en general como para el desarrollo de tratamientos específicos contra enfermedades crónicas.
Estructura y función de la mitocondria
- Visión general de la morfología mitocondrial
Las mitocondrias son orgánulos celulares de apariencia alargada u ovalada, cuyo tamaño puede variar aproximadamente entre 0,5 y 10 micras de longitud.
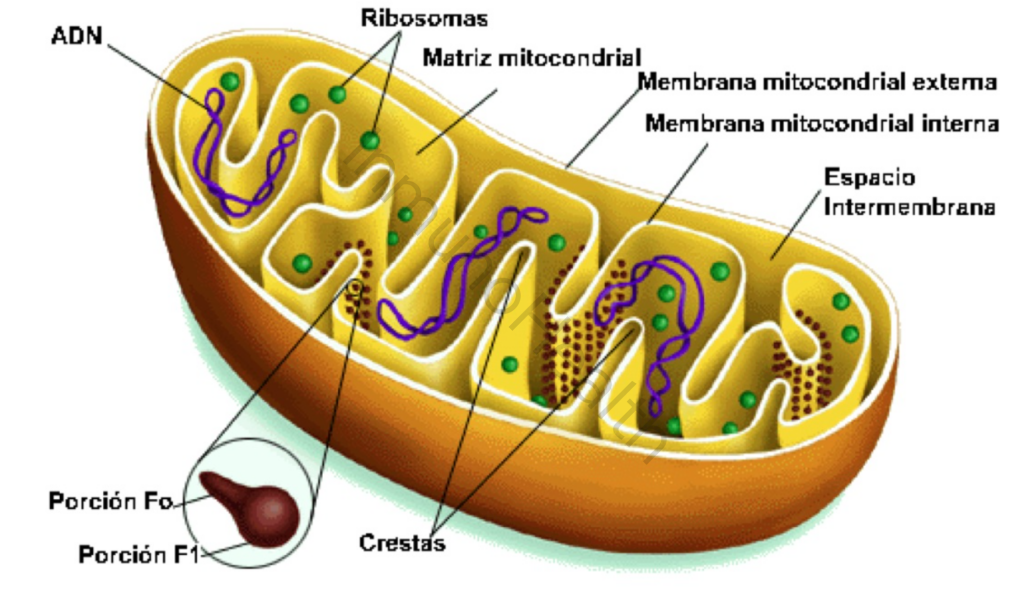
Al observarlas con microscopía electrónica, se aprecia que presentan dos membranas concéntricas: una membrana externa lisa y una membrana interna muy plegada en estructuras llamadas crestas mitocondriales.
Esta organización crea dos espacios diferenciados: el espacio intermembrana (entre las dos membranas) y la matriz mitocondrial (al interior de la membrana interna).
La forma de la mitocondria no es estática; varía en respuesta a las necesidades energéticas de la célula, la disponibilidad de nutrientes y señales celulares.
Además, pueden fusionarse entre sí (fusión mitocondrial) para formar redes más grandes, o fragmentarse (fisión mitocondrial) para adaptarse a condiciones de estrés o para participar en procesos de renovación y eliminación de mitocondrias dañadas.
- La doble membrana y sus propiedades
La membrana externa de la mitocondria contiene porinas, que son proteínas que actúan como canales permitiendo el paso de moléculas relativamente pequeñas. Esto hace que el espacio intermembrana sea químicamente parecido al citosol en términos de concentración de iones y metabolitos pequeños.
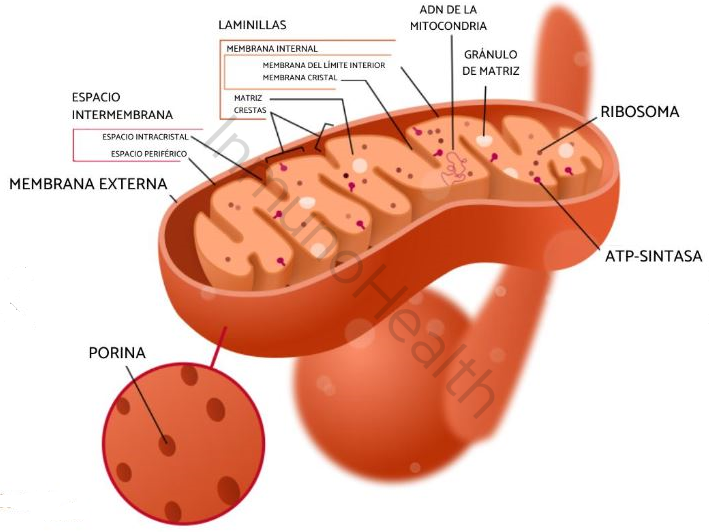
Por su parte, la membrana interna es altamente selectiva y rica en proteínas relacionadas con el transporte de electrones y la producción de ATP.
Su superficie interna se pliega en crestas para aumentar el área donde se ubican los complejos de la cadena de transporte de electrones (CTE) y laP sintasa.
Esta membrana es esencialmente impermeable a iones como el H+, lo que permite la generación de un gradiente electroquímico que resulta fundamental para la fosforilación oxidativa.
- La matriz mitocondrial y su contenido
La matriz es el espacio interno limitado por la membrana interna. Aquí tienen lugar muchas reacciones metabólicas cruciales, como el ciclo del ácido cítrico (ciclo de Krebs) y la β-oxidación de ácidos grasos.
La matriz también contiene enzimas específicas, ribosomas mitocondriales y copias de ADN mitocondrial. Además, en la matriz se hallan concentraciones importantes de NAD+ y FAD, coenzimas indispensables para la recolección de electrones y su posterior paso a la CTE.
- El ADN mitocondrial
- Una de las particularidades más fascinantes de la mitocondria es que posee su propio ADN (mtADN), distinto al ADN nuclear de la célula.
Este ADN mitocondrial es circular, similar al ADN bacteriano, y codifica para un número limitado de proteínas, en su mayoría relacionadas con la cadena de transporte de electrones y la fosforilación oxidativa.
Aun así, la mayor parte de las proteínas mitocondriales son codificadas por el genoma nuclear y se importan al interior del orgánulo.
El mtADN, a diferencia del ADN nuclear, se hereda casi exclusivamente por vía materna. Esto ha permitido usarlo como herramienta en estudios de evolución y parentesco.
Además, su localización en un entorno donde se generan gran cantidad de radicales libres lo hace más susceptible a mutaciones, lo que puede derivar en patologías asociadas a disfunciones mitocondriales.
El papel fundamental de la mitocondria en la célula
- Síntesis de ATP y el concepto de “moneda energética”
La mitocondria se encarga de producir la principal fuente de energía de nuestras células: el ATP. Podemos imaginar el ATP como la “moneda” que permite pagar todos los procesos que requieren energía, como mover los músculos, enviar señales nerviosas o fabricar proteínas.
Cuando el ATP se “rompe” (hidroliza) para liberar energía, se convierte en ADP y fosfato, y así se pueden realizar las distintas funciones celulares.
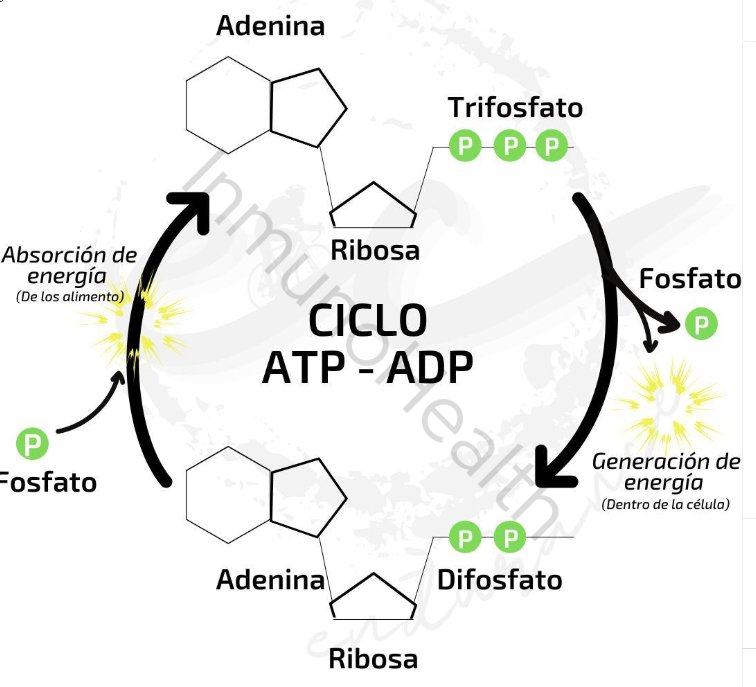
.
- Metabolismo de lípidos y aminoácidos
Aunque solemos pensar que la glucosa es la principal fuente de energía, la mitocondria también usa grasas (a través de un proceso llamado
β-oxidación) y algunos aminoácidos (fragmentos de proteínas) para generar energía.
De esta manera, no sólo produce ATP, sino que también sirve como un centro de intercambio de diferentes rutas metabólicas.
- Apoptosis y señales celulares
Además de fabricar energía, la mitocondria ayuda a regular cuándo una célula debe “retirarse” si está dañada o envejecida, algo que se conoce como apoptosis o “muerte celular programada”.
Si detecta problemas graves, la mitocondria libera señales que inician un proceso ordenado para deshacerse de esa célula y así proteger al organismo de daños mayores.
Los fundamentos de la producción de energía: respiración celular
El proceso por el cual las células degradan las moléculas de alimento para obtener energía recibe el nombre de respiración celular .
La respiración celular es una reacción exergónica, donde parte de la energía contenida en las moléculas de alimento es utilizada por la célula para sintetizar ATP. Decimos parte de la energía porque no toda es utilizada, sino que una parte se pierde.
Para entender cómo logramos grandes cantidades de ATP, veamos los pasos previos que ocurren fuera y dentro de la mitocondria:
La glucólisis: el primer paso en la obtención de energía
La glucólisis es el proceso inicial que las células usan para generar energía a partir de la glucosa, que es un tipo de azúcar. Este proceso ocurre dentro del citoplasma de la célula (el líquido que rodea los pequeños componentes internos llamados orgánulos).
En este paso, una molécula de glucosa (que tiene 6 carbonos) se rompe en dos partes más pequeñas llamadas piruvato, cada una con 3 carbonos.
Durante esta descomposición, se libera un poco de energía en forma de ATP (el «combustible» que usan las células) y también se generan unas moléculas llamadas NADH, que transportan electrones con alta que serán utilizados más adelante en la mitocondria.
Este proceso es crucial para que las células puedan obtener energía rápidamente. Es como romper un gran trozo de azúcar en partes más pequeñas para liberar energía que puede ser usada de inmediato o enviada a las mitocondrias para producir aún más energía, dependiendo de si hay oxígeno o no, tal y como se vera mas adelante.
Aunque el término «glucólisis» suena sencillo, este proceso está compuesto por diferentes etapas químicas, donde se llevan a cabo reacciones específicas con la ayuda de enzimas. Estas etapas son importantes para garantizar que la glucosa se descomponga de manera controlada, pero su explicación es bastante compleja y excede el contenido de esta web.
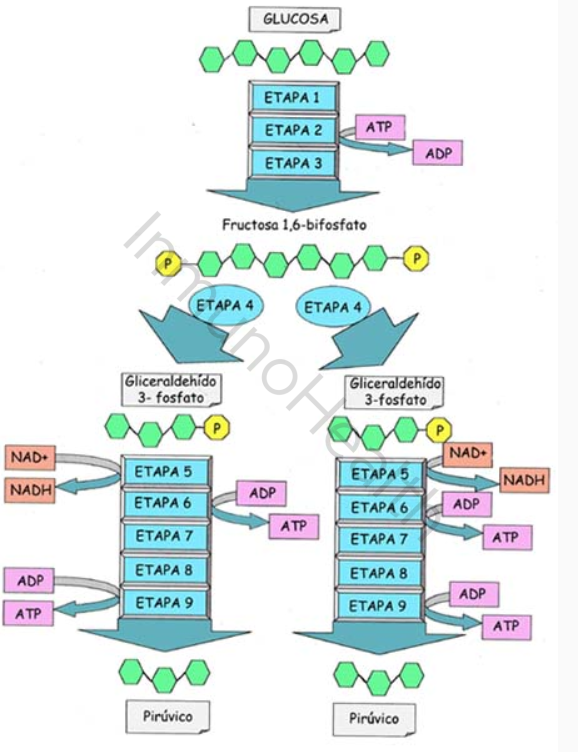
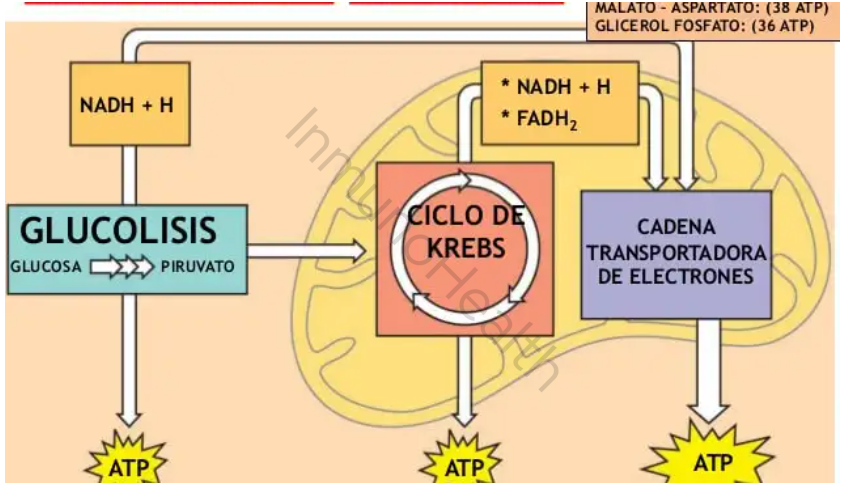
Tal y como se puede ver en la figura de arriba, de cada molécula de glucosa se obtienen dos moléculas de piruvato, un poco de ATP y electrones “de alta energía” que viajan en el NADH.
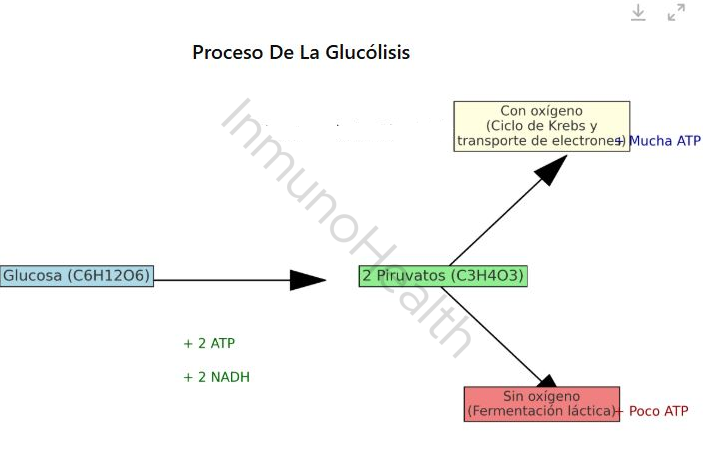
Después de producirse el piruvato, lo que ocurre depende de si hay suficiente oxígeno disponible:
- Sin oxígeno (Vía anaeróbica):
- La glucólisis no necesita oxígeno para funcionar, lo cual es muy útil cuando el oxígeno escasea (como cuando hacemos ejercicio intenso).
- Si no hay oxígeno, el piruvato se transforma en el citoplasma de la célula.en otra molécula llamada lactato (este proceso se conoce como fermentación láctica).
- Aunque no produce mucha energía ATP, permite la regeneración de NAD⁺, una molécula esencial para que la glucólisis pueda continuar, permitIendo que la glucólisis siga funcionando y la célula obtenga al menos un poco de energía.
- Con oxígeno (Más energía):
- Si hay oxígeno, el piruvato entra en las mitocondrias, que son las «centrales energéticas» de las células.
- Allí, el piruvato pasa por otros procesos, como el Ciclo de Krebs y la cadena de transporte de electrones, que generan mucha más energía en forma de ATP, tal y como se explica a continuación.
Una vez formada en la glucólisis, cada molécula de piruvato formada con oxigeno entra en la mitocondria y se convierte en acetil-CoA gracias a un complejo enzimático especial (piruvato deshidrogenasa).
En este proceso se libera dióxido de carbono (CO2) y se generan más electrones de alta energía (NADH). El acetil-CoA alimenta la siguiente etapa del proceso.
El Ciclo de Krebs (Ciclo del Ácido Cítrico)
Después de que la glucólisis rompe una molécula de glucosa en dos moléculas de piruvato, comienza la siguiente etapa para obtener energía: el Ciclo de Krebs, también conocido como el ciclo del ácido cítrico.
Este proceso ocurre dentro de las mitocondrias, que son como pequeñas fábricas de energía en nuestras células. A diferencia de la glucólisis, el Ciclo de Krebs necesita oxígeno para funcionar correctamente.
El Ciclo de Krebs es una serie de reacciones químicas en las que el piruvato, que viene de la glucólisis, se procesa para liberar energía almacenada en sus enlaces químicos. Es como una maquinaria que extrae toda la energía posible de cada molécula.
Como ya se ha mencionado anteriormente, antes de que el piruvato entre en el ciclo, se convierte en una molécula llamada acetil-CoA, que es la verdadera entrada al Ciclo de Krebs. Este proceso también libera una pequeña cantidad de dióxido de carbono (CO₂), que luego eliminamos al respirar.
Una vez que el acetil-CoA entra en el ciclo, se une a una molécula llamada oxaloacetato, formando una nueva molécula llamada citrato (de ahí el nombre «ciclo del ácido cítrico»). A partir de aquí, se producen una serie de pasos en los que se rompen y reorganizan los átomos, liberando energía y más CO₂.
En cada vuelta del ciclo, se generan:
- ATP:
Es la moneda de energía que las células usan directamente.
- NADH y FADH2:
Estas son moléculas que llevan electrones llenos de energía hacia el próximo paso en la producción de energía.
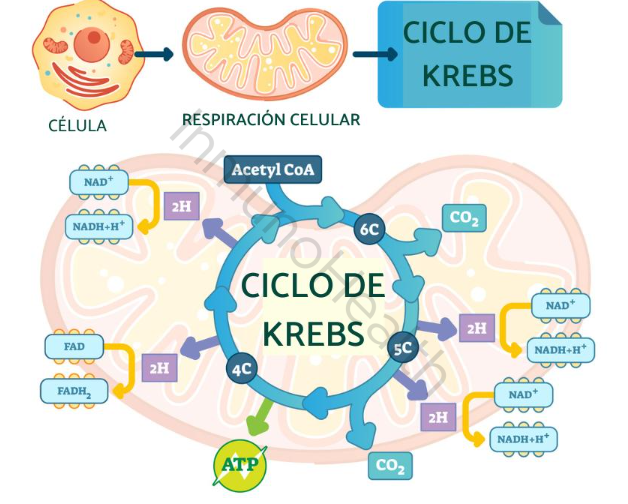
Aunque el Ciclo de Krebs por sí solo produce algo de ATP, su verdadera función es generar grandes cantidades de NADH y FADH2, que luego se usarán en la última etapa del proceso energético: la cadena de transporte de electrones.
Este ciclo es crucial porque permite que las células obtengan la máxima cantidad de energía de cada molécula de glucosa. Sin él, no podríamos producir suficiente energía para mantener procesos básicos como el movimiento, la digestión o incluso pensar.
Sumando la glucólisis y el ciclo de Krebs, de una molécula de glucosa se obtienen 6 moléculas de CO2 (que exhalamos al respirar) y muchos NADH y FADH2.
El NADH y el FADH2 son moléculas que actúan como «camiones de carga» en las células, llevando electrones cargados de energía.
- NADH:
Se produce en la glucólisis y el Ciclo de Krebs, y transporta más energía.
- FADH2:
También se genera en el Ciclo de Krebs, pero transporta un poco menos de energía que el NADH.
Ambas entregan esta energía a la cadena de transporte de electrones, donde se convierte en ATP, que es el combustible que las células usan para funcionar. Sin estas moléculas, las células no podrían producir suficiente energía para vivir.
La Cadena de Transporte de Electrones o Fosforilación Oxidativa: La Fábrica Final de Energía
Después del Ciclo de Krebs, todavía queda un paso crucial para que las células obtengan la máxima energía de los alimentos que comemos.
Este paso se llama la Fosforilación Oxidativa o Cadena de Transporte de Electrones (CTE) y es la última etapa de un proceso increíble que ocurre en nuestras células para generar energía, algo esencial para que podamos movernos, pensar, e incluso respirar.
Aquí es donde ocurre la magia. Los electrones generados en las fases anteriores se transportan a lo largo de la cadena de transporte de electrones en la membrana mitocondrial interna. Esta transferencia de electrones impulsa la producción de ATP mediante la enzima ATP sintasa. Al final del proceso, el oxígeno actúa como receptor final de electrones, formando agua como subproducto.
Este paso viene después del ciclo de Krebs y se lleva a cabo en las mitocondrias, que son como las fábricas de energía dentro de nuestras células.
Gracias al CTE, nuestro cuerpo convierte la energía química de los alimentos en una forma que nuestras células pueden usar: el ATP (adenosín trifosfato).
El CTE es un proceso donde los electrones, partículas cargadas de energía, se mueven a través de una serie de proteínas especiales. Estas proteínas están incrustadas en la membrana interna de las mitocondrias y trabajan juntas para liberar energía y almacenarla en forma de ATP, que las células usan como fuente de energía para realizar cualquier función.
Tal y como hemos visto, el proceso comienza durante el ciclo de Krebs, con la formacion de moléculas especiales que liberan su energía, como la NADH y FADH2. Estas moléculas actúan como «portadores de energía», entregando electrones al CTE.
Aquí está lo que sucede:
- Transferencia de electrones:
Los electrones de NADH y FADH2 se pasan de una proteína a otra dentro de la membrana interna de la mitocondria. Estas proteínas actúan como «escalones» que ayudan a mover los electrones. - Bombeo de protones:
A medida que los electrones se mueven por la cadena, liberan energía. Esta energía se usa para bombear protones (pequeñas partículas cargadas positivamente) desde el interior de la mitocondria hacia el espacio entre las membranas. Esto crea un gradiente, como si se acumulara agua detrás de una presa. - Generación de ATP:
Los protones quieren volver al interior de la mitocondria, y lo hacen a través de una proteína especial llamada ATP sintasa. Este movimiento libera energía que la ATP sintasa utiliza para fabricar ATP. Es como un molino de agua que gira cuando los protones fluyen y produce energía. - Producción de agua:
Al final del proceso, los electrones se combinan con oxígeno y protones para formar agua. Por eso el oxígeno que respiramos es tan importante; sin él, este sistema no funcionaría.
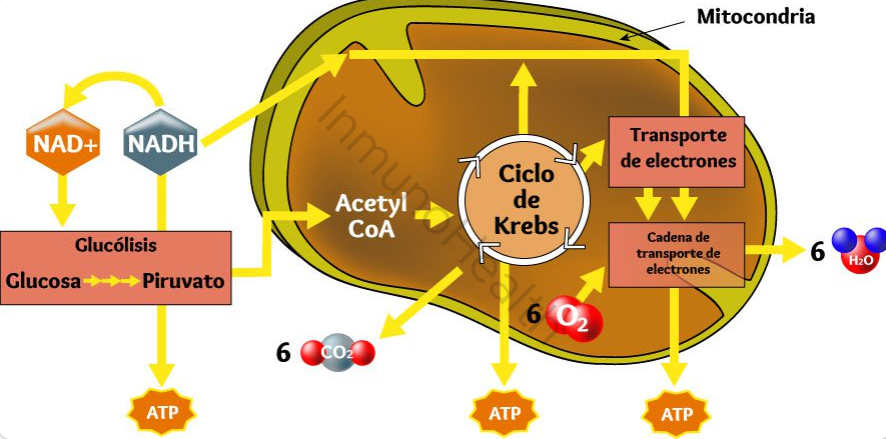
La CTE es el paso más eficiente en la producción de energía. Por cada molécula de glucosa que comenzó en la glucólisis, la CTE puede generar hasta 34 moléculas de ATP de las 38 moleculas que se pueden generar a partir de una molécula de glucosa,
Cada molécula de ATP (adenosín trifosfato) almacena aproximadamente 7,3 kilocalorías (kcal) de energía cuando se hidroliza en condiciones estándar (es decir, cuando se rompe uno de sus enlaces de fosfato, convirtiéndose en ADP y fosfato inorgánico).
El Estrés Oxidativo: El Enemigo Silencioso de las Mitocondrias
El proceso descrito anteriormente para la producción de energía y respiración celular no está exento de riesgos. Durante la fosforilación oxidativa o Cadena de Transporte de Electrones (CTE), las mitocondrias generan especies reactivas de oxígeno (ROS), también conocidas como radicales libres.
Aunque en pequeñas cantidades estas moléculas desempeñan funciones biológicas útiles, su acumulación puede dañar la estructura y el funcionamiento mitocondrial, un fenómeno conocido como estrés oxidativo.
El estrés oxidativo es un fenómeno biológico que ocurre cuando hay un desequilibrio entre la producción de radicales libres y la capacidad del cuerpo para neutralizarlos mediante antioxidantes.
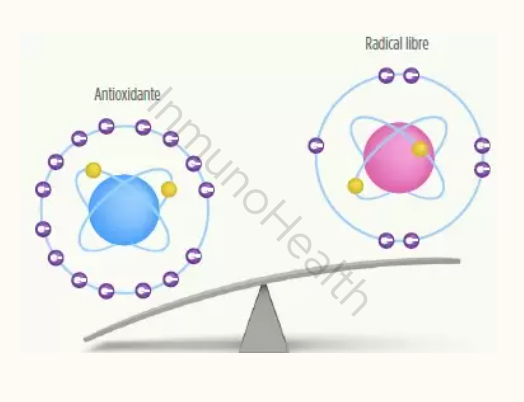
Los radicales libres son moléculas inestables que se generan como subproductos naturales del metabolismo celular y pueden incrementarse por factores externos como la contaminación, el tabaquismo, la radiación ultravioleta y una dieta poco saludable.
En un próximo capitulo se hara un análisis detallado sobre los radicales libres, porque se producen, los tipos de radicales libres que hay y los efectos nocivos que producen en la salud.
El estrés oxidativo mitocondrial
Las mitocondrias, conocidas como las «centrales energéticas» de las células, son especialmente vulnerables al estrés oxidativo ya que cuando los radicales libres superan la capacidad del cuerpo para neutralizarlos, las mitocondrias comienzan a deteriorarse de forma relevante.
Como ya se ha visto en detalle en el apartado anterior, estas estructuras producen energía en forma de ATP (adenosín trifosfato) mediante un proceso llamado fosforilación oxidativa o Cadena de Transporte de Electrones (CTE).
Durante este proceso, las mitocondrias generan pequeñas cantidades de especies reactivas de oxígeno (ROS), también conocidas como radicales libres como subproducto. Si estos radicales libres no se neutralizan adecuadamente, pueden causar daño a los componentes mitocondriales esenciales tales como:
- Lípidos:
Afectan las membranas mitocondriales.
- Proteínas:
Deterioran la maquinaria celular.
- ADN mitocondrial:
Alteraciones genéticas que reducen la eficiencia energética.
La disfunción mitocondrial, que resulta del daño causado por el estrés oxidativo, puede desencadenar una amplia gama de problemas de salud, afectando tanto la calidad de vida como la longevidad de las personas.
- Fatiga crónica:
Las mitocondrias son las principales productoras de energía en las células, por lo que cualquier alteración en su función reduce significativamente la capacidad del cuerpo para generar energía.
Esto puede manifestarse como una sensación constante de cansancio extremo, que no mejora con el descanso y limita la capacidad de realizar actividades cotidianas.
- Enfermedades neurodegenerativas:
Las neuronas son altamente dependientes de la energía mitocondrial para mantener sus funciones. La acumulación de daño mitocondrial puede contribuir al desarrollo de enfermedades como el Alzhéimer y el Parkinson, caracterizadas por la degeneración progresiva del sistema nervioso. Estos trastornos afectan la memoria, la coordinación y otras funciones esenciales.
- Cáncer:
La disfunción mitocondrial puede influir en la aparición y progresión del cáncer al alterar el metabolismo celular y favorecer un ambiente propicio para la proliferación descontrolada de células malignas. Además, el daño al ADN mitocondrial puede generar mutaciones que aumentan el riesgo de formación de tumores.
- Trastornos metabólicos:
Enfermedades como la diabetes están directamente relacionadas con la capacidad de las células para regular el metabolismo energético. Cuando las mitocondrias no funcionan correctamente, el equilibrio en la producción y utilización de glucosa e insulina se ve afectado, lo que contribuye al desarrollo y progresión de este trastorno metabólico.
Estas consecuencias subrayan la importancia de proteger la salud mitocondrial para prevenir el desarrollo de enfermedades crónicas y mejorar la calidad de vida.
Promover hábitos saludables, controlar los niveles de estrés oxidativo y garantizar una dieta adecuada son pasos fundamentales para preservar la función mitocondrial.

Para combatir el estrés oxidativo, el cuerpo utiliza un sistema de defensa compuesto por antioxidantes, que son moléculas capaces de neutralizar los radicales libres y prevenir el daño celular, actuando como escudos protectores, impidiendo que los radicales libres, que son moléculas inestables y altamente reactivas, dañen estructuras esenciales como las membranas celulares, el ADN y las proteínas.
Entre los antioxidantes más importantes se encuentran las vitaminas C y E, el betacaroteno, los polifenoles y ciertos minerales como el selenio. Sin embargo, el glutatión destaca como el antioxidante maestro del organismo
En el siguiente apartado se detalla el papel esencial del glutatión en la salud mitocondrial, explicando cómo protege estas estructuras del estrés oxidativo, preserva su funcionalidad en la producción de energía y previene daños en el ADN mitocondrial.
Además, se abordarán estrategias para mantener niveles óptimos de glutatión y su impacto en la prevención de enfermedades relacionadas con la disfunción mitocondrial.
La Importancia del Glutatión como Protector Mitocondrial y Energizador
El Glutatión desempeña un papel crucial en la protección y el correcto funcionamiento de las mitocondrias, los «motores energéticos» de nuestras células.
Tal y como se ha visto en los anteriores apartados, las mitocondrias son esenciales para producir ATP, la principal fuente de energía para las funciones biológicas, pero son altamente vulnerables al daño oxidativo debido a la generación constante de radicales libres durante el proceso de producción de energía.
Aquí es donde el glutatión, como antioxidante maestro, entra en acción, actuando como protector mitocondrial y estabilizador energético.
Protección Mitocondrial y Función Energética
La capacidad del glutatión para neutralizar especies reactivas de oxígeno (ROS) es fundamental para preservar la integridad mitocondrial.
Los ROS son subproductos inevitables del metabolismo energético mitocondrial. Tal y como se ha indicado anteriormente, si no se controlan, estas moléculas pueden dañar lípidos, proteínas y ADN mitocondrial, lo que resulta en disfunción mitocondrial y, en casos graves, apoptosis celular, que dada su capacidad acumulativa, puede conllevar envejecimiento celular y al desarrollo de enfermedades crónicas, como el cáncer, las enfermedades neurodegenerativas y las patologías cardiovasculares.
El glutatión, una pequeña molécula antioxidante, juega un papel crucial en la neutralización de estas especies reactivas actuando como una barrera crítica contra este daño oxidativo.
Su forma reducida (GSH) se encuentra en altas concentraciones en las mitocondrias, donde neutraliza las ROS al donar un electrón, convirtiéndolas en formas menos reactivas.
Además, el glutatión puede regenerarse a través de enzimas como la glutatión reductasa, asegurando una defensa antioxidante sostenida. Sin esta protección, las mitocondrias se enfrentan a un desgaste acelerado, comprometiendo su capacidad para generar energía de manera eficiente.
Consecuencias de Niveles Bajos de Glutatión en las Mitocondrias
Cuando los niveles de glutatión disminuyen, las mitocondrias se vuelven vulnerables al estrés oxidativo, lo que desencadena una serie de problemas interrelacionados, tal y como se describen a continuación:
- Disfunción Mitocondrial
El daño oxidativo afecta componentes esenciales de las mitocondrias, como las proteínas de la cadena respiratoria. Esto resulta en una menor producción de ATP, que se traduce en fatiga celular y un funcionamiento deficiente de órganos y tejidos.
Enfermedades como la diabetes tipo 2, la fibromialgia y el síndrome de fatiga crónica están estrechamente relacionadas con esta disfunción.
- Aumento de la Apoptosis
El daño mitocondrial crónico puede activar mecanismos de apoptosis, o muerte celular programada. Esto no solo contribuye a la degeneración tisular, sino que también afecta la regeneración celular, exacerbando enfermedades neurodegenerativas como el Alzheimer y el Parkinson.
- Disminución de la Energía Celular
La energía insuficiente se manifiesta como fatiga persistente, disminución del rendimiento físico y mental, y menor capacidad para recuperarse de enfermedades o lesiones. En atletas y personas activas, esto puede limitar el desempeño y aumentar el riesgo de lesiones.
- Mayor Susceptibilidad a Enfermedades Crónicas
La falta de glutatión deja a las células sin protección frente a agentes dañinos, lo que incrementa el riesgo de enfermedades autoinmunes, cardiovasculares y oncológicas.
Factores que Contribuyen a la Reducción del Glutatión Mitocondrial
El glutatión puede disminuir o agotarse debido a diversos factores, los cuales incluyen una amplia variedad de causas tanto internas como externas que afectan directamente su síntesis y disponibilidad en el organismo.
Entre los factores que contribuyen a su reducción están los siguientes:
- Estrés Crónico
El estrés activa el eje hipotalámico-hipofisario-adrenal, aumentando los niveles de cortisol. Este proceso genera ROS adicionales que consumen las reservas de glutatión, dejando a las células más expuestas al daño oxidativo.
- Dieta Deficiente
La síntesis de glutatión requiere aminoácidos como cisteína, glicina y glutamato. Una dieta pobre en proteínas de alta calidad y vegetales ricos en compuestos sulfurosos afecta directamente la capacidad del cuerpo para producir glutatión.
- Exposición a Toxinas
Los contaminantes ambientales, metales pesados, pesticidas y otras toxinas aumentan la carga oxidativa en las células, exigiendo mayores cantidades de glutatión para su neutralización. Esto agota rápidamente las reservas disponibles.
- Enfermedades Crónicas
Enfermedades como el cáncer, las infecciones virales crónicas y los trastornos metabólicos aumentan el consumo de glutatión, dejando menos disponible para las funciones normales de las mitocondrias.
- Envejecimiento
Con la edad, la capacidad natural del cuerpo para producir y reciclar glutatión disminuye, lo que explica en parte el aumento del daño oxidativo y la disminución de la energía en personas mayores.
Beneficios del Glutatión en la Salud Mitocondrial
Conservar niveles óptimos de glutatión es esencial para la salud mitocondrial, ya que este antioxidante desempeña un papel clave en la protección de las mitocondrias frente al estrés oxidativo, asegurando su funcionalidad y capacidad para producir energía de manera eficiente.
Al actuar como un estabilizador del equilibrio redox, el glutatión permite también que las mitocondrias generen ATP de forma sostenida
Los beneficios del Glutatión para mantener una correcta salud mitocondrial serían las siguientes:
- Mejora de la Producción de Energía
Un entorno mitocondrial protegido garantiza una producción eficiente de ATP, lo que se traduce en niveles de energía estables y sostenidos. Esto es crucial tanto para la vitalidad diaria como para el rendimiento deportivo.
- Protección del ADN Mitocondrial
El ADN mitocondrial es más vulnerable al daño oxidativo que el ADN nuclear. El glutatión previene mutaciones y errores que pueden comprometer la función mitocondrial a largo plazo.
- Reducción del Riesgo de Enfermedades Degenerativas
Un balance redox saludable reduce significativamente la inflamación crónica y protege contra enfermedades como la aterosclerosis, el Alzheimer y el Parkinson.
- Apoyo al Sistema Inmune
Las células inmunes dependen de mitocondrias funcionales para responder adecuadamente a infecciones y lesiones. El glutatión asegura su eficiencia, mejorando la capacidad del cuerpo para combatir enfermedades.
- Mitigación del Envejecimiento Celular
La protección antioxidante que ofrece el glutatión retrasa los signos del envejecimiento, preservando la funcionalidad celular y la vitalidad física.
Estrategias para Optimizar los Niveles de Glutatión
Para mantener niveles óptimos de glutatión en el organismo, es esencial adoptar ciertos hábitos saludables y evitar conductas que puedan disminuir sus reservas.
A continuación, se vuelve a presenta la tabla que detalla las recomendaciones clave para preservar este antioxidante maestro, que ya fue mostrada y explicada en el capitulo correspondiente al Refuerzo del Sistema Inmune (I):
| QUE HACER | QUE NO HACER |
| Consumir una dieta en precursores de Glutatión y antioxidantes como vitaminas C y E asi como rica en minerales (zink, selenio, etc..), que incluye alimentos como ajo, cebolla, brócoli, espinacas y frutas cítricas | Evitar dietas altas en azúcar, grasas trans y alimentos ultraprocesados. |
| Suplementarse con precursores de glutation como Proteina de Suero, N-acetilcisteína (NAC) que son precursores efectivo del glutatión. Otros suplementos, como el ácido alfa-lipoico y las vitaminas C y E, también contribuyen al reciclaje del glutatión. | Considerar que la suplementacion con precursores no es efectiva |
| Beber suficiente agua para mantener una buena hidratación. | No fumar, ya que el tabaco daña el sistema respiratorio e inmunitario. |
| Dormir de 7 a 9 horas cada noche. | No abusar del alcohol, ya que debilita las células inmunitarias. |
| Hacer ejercicio moderado regularmente (caminar, nadar, yoga, etc.). | Evitar el sedentarismo o la inactividad prolongada. |
| Reducir el estrés con técnicas como meditación o mindfulness. | No ignorar el estrés crónico, ya que suprime la inmunidad. |
| Mantener una buena higiene personal (lavarse las manos, limpiar superficies). | No descuidar la higiene, especialmente en contacto con personas infectadas. |
| Vacunarse según las recomendaciones médicas. | No saltarse las vacunas o ignorar su importancia en la prevención de infecciones. |
| Consumir probióticos para mejorar la microbiota intestinal. | Evitar el uso innecesario de antibióticos que alteran la flora intestinal. |
| Protegerse de toxinas ambientales y contaminantes químicos. | No exponerse de forma prolongada a pesticidas y productos químicos dañinos. |
| Consultar al médico regularmente para chequeos preventivos. | No ignorar síntomas ni posponer revisiones médicas importantes. |
Ensayos Clínicos: Glutatión, Producción de Energía y Salud Mitocondrial
En los últimos años se han publicado muchos ensayos clínicos en PubMed los cuales destacan la importancia del glutatión en la producción de energía celular asi como en la mejora en la salud mitocondrial , evidenciando su papel crucial en la regulación del equilibrio redox dentro de las mitocondrias y en la protección contra el daño oxidativo.
Estos estudios han demostrado que niveles adecuados de glutatión favorecen una mayor eficiencia en la generación de ATP, reducen la acumulación de especies reactivas de oxígeno y previenen la disfunción mitocondrial, factores clave para mantener la vitalidad celular y prevenir enfermedades relacionadas con el deterioro mitocondrial, como las neurodegenerativas y metabólicas.
A continuación, se presenta una selección de 20 estudios científicos relevantes que respaldan su papel terapéutico y preventivo, publicados en diferentes revistas especializadas :
- Glutathione: Overview of its protective roles, measurement, and biosynthesis
Autores: Dean P. Jones, Patricia E. Carlson.
Revista: Molecular Aspects of Medicine, 1998
Resumen: Este artículo revisa las funciones protectoras del glutatión, su medición y biosíntesis, destacando su importancia en la defensa antioxidante y en la regulación del estado redox celular, fundamentales para la producción de energía y la salud mitocondrial.
- Glutathione and mitochondria: beyond an antioxidant
Autores: Giuseppe Filomeni, Daniele De Zio, Francesco Cecconi
Revista: Biochimica et Biophysica Acta (BBA) – Bioenergetics, 2015
Resumen: El estudio explora cómo el glutatión regula funciones mitocondriales más allá de su papel antioxidante, incluyendo la modulación de la biogénesis mitocondrial y la apoptosis, lo que impacta en la producción de energía celular.
- Mitochondrial glutathione: features, regulation and role in disease
Autores: Stefan H. H. van der Vliet, Paul S. Brookes
Revista: Biochimica et Biophysica Acta (BBA) – Molecular Basis of Disease, 2008
Resumen: Este artículo revisa las características del glutatión mitocondrial, su regulación y su papel en diversas enfermedades, enfatizando su importancia en la protección contra el estrés oxidativo y en la función energética mitocondrial.
- Glutathione and mitochondrial function in aging and neurodegeneration
Autores: D. Allan Butterfield, Christopher M. Reed
Revista: Free Radical Biology and Medicine, 2016
Resumen: El estudio analiza la relación entre el glutatión y la función mitocondrial en el envejecimiento y las enfermedades neurodegenerativas, sugiriendo que la disminución de glutatión contribuye a la disfunción mitocondrial y al deterioro energético.
- Glutathione: a key player in neuroprotection and redox signaling
Autores: José M. Mato, Shelly C. Lu
Revista: Neurochemical Research, 2007
Resumen: Este artículo destaca el papel del glutatión en la neuroprotección y la señalización redox, subrayando su importancia en la regulación de la función mitocondrial y la producción de energía en células neuronales.
- Glutathione and mitochondria in cardiac disease
Autores: Rajasekaran Namakkal-Soorappan, Natarajan Venkatachalam
Revista: Current Opinion in Clinical Nutrition and Metabolic Care, 2012
Resumen: El estudio revisa la interacción entre el glutatión y las mitocondrias en enfermedades cardíacas, indicando cómo el equilibrio del glutatión es crucial para mantener la función mitocondrial y la producción de energía en el corazón.
- Glutathione and mitochondrial DNA mutations in human disease
Autores: Douglas C. Wallace, Richard A. Cooper
Revista: Proceedings of the National Academy of Sciences, 1985
Resumen: El estudio investiga la relación entre el glutatión y las mutaciones del ADN mitocondrial en enfermedades humanas, sugiriendo que el glutatión puede influir en la estabilidad genética mitocondrial y en la producción de energía.
- Glutathione and mitochondrial thiol redox control in neurodegeneration
Autores: J. Timothy Greenamyre, Robert C. Parker
Revista: Neuroscientist, 1995
Resumen: Este artículo revisa el papel del glutatión y el control redox de los tioles mitocondriales en la neurodegeneración, destacando su importancia en la producción de energía y la supervivencia neuronal.
- Glutathione and mitochondrial oxidative stress in neurodegenerative disorders
Autores: Jeffrey M. Gutterman, Mark P. Mattson
Revista: Annals of the New York Academy of Sciences, 2001
Resumen: El estudio analiza cómo el glutatión mitocondrial modula el estrés oxidativo en trastornos neurodegenerativos, afectando la función mitocondrial y la producción de energía celular.
- Mechanism of glutathione production in neurons
Autores: Nobuko Matsumura, Chisato Kinoshita, Koji Aoyama
Publicado en: Nihon Yakurigaku Zasshi, 2021
Resumen: Este estudio analiza cómo la disfunción del transportador EAAC1 reduce los niveles de glutatión en el cerebro, influyendo en la neurodegeneración. Propone que inhibidores de miR-96-5p podrían aumentar la producción neuronal de glutatión, ofreciendo una vía para prevenir enfermedades neurodegenerativas.
- Glutathione and Mitochondrial Function in Sepsis
Autores: Greg S. Martin, Craig M. Coopersmith
Revista: Shock, 2009
Resumen: Este artículo explora la relación entre el glutatión y la función mitocondrial en la sepsis, sugiriendo que la modulación de los niveles de glutatión puede influir en la bioenergética mitocondrial y en la respuesta inflamatoria durante la sepsis
- Mitochondrial Glutathione in Cellular Redox Homeostasis and Apoptosis
Autores: Yingying Wu, Yifan Zhang, Xiaodong Wang
Revista: International Journal of Molecular Sciences, 2021
Resumen: Este estudio analiza cómo el glutatión mitocondrial (mGSH) metaboliza el peróxido de hidrógeno dentro de las mitocondrias, y cómo un desequilibrio prolongado entre las especies reactivas de oxígeno y el mGSH puede conducir a disfunción celular y apoptosis
- How the Antioxidant Glutathione Keeps Mitochondria Healthy
Autores: Kıvanç Birsoy, et al.
Revista: ScienceDaily, 2023
Resumen: Investigadores descubrieron cómo las mitocondrias detectan y controlan sus niveles de glutatión, un antioxidante producido en todo el cuerpo, revelando el primer mecanismo de detección de nutrientes identificado para un orgánulo, con potenciales aplicaciones en salud.
- Scientists Discover How Mitochondria Import Antioxidants
Autores: Kıvanç Birsoy, et al.
Revista: Rockefeller University News, 2021
Resumen: Este estudio identifica una molécula clave que transporta glutatión, el principal antioxidante del cuerpo, hacia las mitocondrias, donde se producen radicales libres en masa, abriendo nuevas posibilidades para investigar el estrés oxidativo y sus efectos dañinos.
- Mitochondrial Glutathione, a Key Survival Antioxidant
Autores: María C. Fernández-Checa, José M. García-Ruiz
Revista: CSIC Digital Repository, 2010
Resumen: Este artículo destaca la importancia del glutatión mitocondrial (mGSH) como la principal línea de defensa para mantener el ambiente redox mitocondrial adecuado, evitando modificaciones oxidativas que conducen a disfunción mitocondrial y muerte celular


